铀(U)
铀,是元素周期表中第七周期MB族元素,锕系元素之一,原子序数92,原子量238.0289,是最重要的核燃料,元素名源于纪念1781年发现的天王星“Uranus”。是致密而有延展性的银白色放射性金属。铀在接近绝对零度时有超导性,有延展性。铀的化学性质活泼,易与绝大多数非金属反应,能与多种金属形成合金。铀最初只用做玻璃着色或陶瓷釉料,1938年发现铀核裂变后,开始成为主要的核原料。1789年德国化学家克拉普罗特从沥青铀矿中发现铀的氧化物。1841年法国化学家佩利若用钾还原四氯化铀制的金属铀。
铀原子有92个质子和92个电子,其中6个是价电子。铀是银白色金属,熔点1132.5℃,沸点3745℃,密度18.95g/cm3,抗拉强度450MPa,屈服强度207MPa,弹性模数172GPa。铀在接近绝对零度时有超导性,有延展性。
铀的外电子层构型为5f36dl7s2,有+3,+4,+5,+6四种价态,其中+4和+6价化合物稳定。铀的化学性质活泼,能和所有的非金属作用(惰性气体除外),能与多种金属形成合金。空气中易氧化,生成一层发暗的氧化膜,高度粉碎的铀空气中极易自燃,块状铀在空气中易氧化失去金属光泽,在空气中加热即燃烧,铀能与所有非金属反应,250℃下和硫反应,400℃下和氮反应生成氮化物,1250℃下和碳反应生成碳化物,250-300℃下和氢反应生成UH3,UH3在真空350-400℃下分解,放出氢气。铀与卤素反应生成卤化物,铀能与汞、锡、铜、铅、铝、铋、铁、镍、锰、钴、锌、铍作用生成金属间化合物,金属铀缓慢溶于硫酸和磷酸,有氧化剂存在时会加速溶解,铀易溶于硝酸,铀对碱性溶液呈惰性,但有氧化剂存在时,能使铀溶解,铀及其化合物均有较大的毒性,空气中可溶性铀化合物的允许浓度为0.05mg/m3,不溶性铀化合物允许浓度为0.25mg/m3,人体对天然铀的放射性允许剂量,可溶性铀化合物为7400Bq,不溶性铀化合物为333Bq。
存在于许多岩石中,但大量只存在于沥青铀矿和钒钾铀矿中。
在自然界中,铀以铀-238(99.2742%)、铀-235(0.7204%)以及极微量的铀-234(0.0054%)等同位素存在。铀衰变时释放出α粒子,过程缓慢,拥有很长的半衰期。铀-238的半衰期约为44.7亿年,铀-235则为7.04亿年,常用于测定地质年代。少量存在于独居石等稀土矿石中。铀是自然元素中质量次重、原子量次高的元素,仅次于钚-244[3]。它的密度比铅高出约70%,但不如金、钨密食。铀在自然界中以数百万分率的低含量存在于土壤、矿石和水中,可借由开采沥青铀矿等含铀矿物并提炼之。
古时候它被用作玻璃颜料,现在用作核反应及核弹燃料。千百年来铀一直被用作给玻璃染色的色素,然而现在纯金属铀是核反应堆和原子弹中使用的核燃料。少量用于电子管制造业中的除氧剂和惰性气体提纯(除氧、氢)。
铀最初只用做玻璃着色或陶瓷釉料,1938年发现铀核裂变后,开始成为主要的核原料。在居里夫妇发现镭以后,由于镭具有治疗癌症的特殊功效,镭的需要量不断增加,因此许多国家开始从沥青铀矿中提炼镭,而提炼过镭的含铀矿渣就堆在一边,成了“废料”。然而,铀核裂变现象发现后,铀变成了最重要的元素之一。这些“废料”也就成了“宝贝”。从此,铀的开采工业大大地发展起来,并迅速地建立起了独立完整的原子能工业体系。 | 元素名称 | 铀 | 元素符号 | U | 原子序数 | 92 | 相对原子质量
(12C=12.0000) | 238.029 | | 英文名称 | Uranium | | 原子结构 | 原子半径(Å) | | 原子体积(cm3/mol) | 12.59 | 电子模型 | 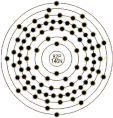
| | 电子构型 | 1s2 2s2p6 3s2p6d10 4s2p6d10f14 5s2p6d10f3 6s2p6d1 7s2 | 离子半径(Å) | 0.52 | | 共价半径(Å) | 0.52 | 氧化态 | 6,5,4,3 | | 发现 | 1789年由 M.J. Klaproth (德国,伯林)发现,1841年由 W.M. Peligot (法国,巴黎)首次作为金属分离出。 | | 命名起源 | after the planet 'Uranus' | | 来源 | 存在于许多岩石中,但大量只存在于沥青铀矿和钒钾铀矿中。 | | 用途 | 古时候它被用作玻璃颜料,现在用作核反应及核弹燃料等。 | | 物理性质 | 状态 | 一个非常重的,银白色放射性金属。 | 熔 点(℃) | 1132 | 沸 点(℃) | 4134 | | 密度(g/cc,300K) | 18.95 | 比 热(J/gK) | 0.12 | 蒸发热(KJ/mol) | 477 | | 熔化热(KJ/mol) | 8.52 | 导电率(106/cm) | 0.038 | 导热系数(W/cmK) | 0.276 | | 自燃点(℃) | - | 闪 点(℃) | - | | | | 化学性质 | | | 地质数据 | 丰 度 | | 滞留时间(年) | 300000 | 太阳
(相对于 H=1×1012) | <4 | | 海水中(ppm) | 3.13×10-3 | 地壳(ppm) | 2.4 | 大西洋表面 | - | | 太平洋表面 | - | 大气(ppm(体积)) | - | 大西洋深处 | - | | 太平洋深处 | - | | | | | | 生物数据 | 人体中含量 | | 肝(ppm) | 0.003 | | 器官中 | | 肌肉(ppm) | 0.0009 | | 血(mg dm-3) | 5×10-4 | 日摄入量(mg) | 0.001-0.002 | | 骨(ppm) | (0.16-70)×10-3 | 人(70Kg)均体内总量(mg) | 0.1 |
铀的同位素信息 | 同位素 | % | 质量 | 自旋 | 核磁矩 | 磁旋比 | Q | 频率 | 吸收率 | | [232] | 0 | 232.037146 | | | | | | | | [233] | 0 | 233.039628 | | | | | | | | [234] | 0.0055 | 234.0409 | | | | | | | | [235] | 0.72 | 235.0439 | 7/2 | -0.43 | -0.52 | 439.6 | 1.8414 | | | [236] | 0 | 236.045561 | | | | | | | | [238] | 99.2745 | 238.050784 | | | | | | |
| |
您可能感兴趣的产品:
|