揭秘分子间“热”对话:等温滴定量热仪如何推动生命科学发现?
作者:瑞科和利 2025.03.07 点击3次
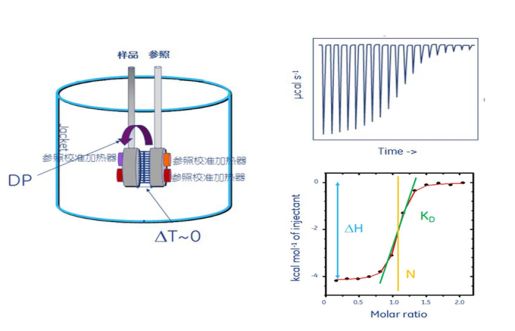
等温滴定量热法(Isothermal titration calorimetry,ITC) 是一种可以直接测量生物过程结合能量的技术,包括蛋白质- 配体结合、蛋白质- 蛋白质结合、DNA- 蛋白质结合、蛋白质- 碳水化合物结合、蛋白质- 脂质结合和抗原- 抗体结合。 ITC 仪器是一个根据动态功率补偿原理工作的热通量热量计,即它测量样品和参比池之间保持恒定温差(接近零)所需的功率量(μcal/sec)。简单地说,就是指将一种反应物配制成澄清溶液放在一个温控样品池中,通过一个热电偶回路与参比池偶联,另一种反应物作为配体置于注射器中。其中,样品池和参比池通过绝热装置隔开,但保持环境条件相同。在恒定温度下,注射器以一定速度向样品池中不断滴加配体,注射器还具有搅拌功能,反应一定时间,仪器测量样品池的热量变化并使其与参比池平衡,显示为一个吸热或放热的峰。放热反应触发恒温功率的负反馈,而吸热反应则触发恒温功率的正反馈来保持温度恒定。反馈系统降低或升高所施加的热功率以补偿这种温度不平衡,每次注射后,系统达到平衡并恢复至恒定温度。因此,记录的信号显示出峰值形式的典型偏转模式(如图1所示)。假设基线作为参考,对滴定峰进行积分,就会得到相关的热量。当样品池中的反应物变得饱和时,热信号减小直至仅背景热。
图1. 等温滴定量热仪的简略工作示意图 等温滴定量热法 (ITC) 是一种高分辨率方法,用于完整表征相互作用的基本化学细节,通过自带软件对滴定结果进行拟合、分析可得到测量热力学性质,包括:相互作用的化学计量学(n)、亲和力常数(KD)、焓变化(∆H)、熵变化(∆S) 、吉布斯自由能(∆G)和恒压摩尔热容(∆Cp)。ITC 测量的是在自然状态下无外力作用的结合伴侣间的亲和力,无需使用荧光标签修饰组分或使样品固定化。 酶的催化动力学及抑制剂研究是酶学研究中非常重要的一个部分,得到的信息能够预测催化反应的路径。等温滴定量热技术作为一种新兴的测定方法,可以快速直接准确测量化学反应过程中产生的热量变化。 广西高校资源化工应用新技术重点实验室廖丹葵课题组利用等温滴定量热仪NANO ITC(TA Instrument))测定肺血管紧张素转化酶(ACE)催化水解其体外模拟底物马尿酰-组氨酰-亮氨酸(HHL)反应的热动力学参数,考察了温度对动力学参数的影响。
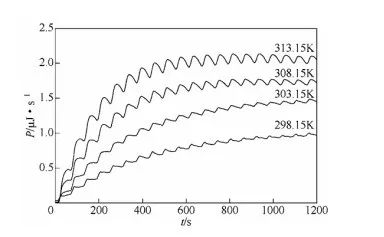
图2.不同温度下ACE催化HHL水解反应的等温 滴定量热曲线
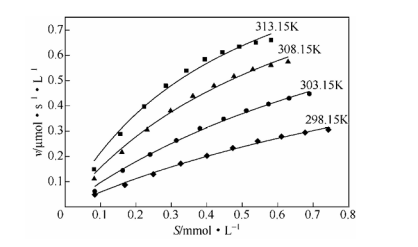
图3.不同温度下ACE酶促反应动力学曲线 结果表明,该反应的摩尔水解焓ΔHhydr为正值,是吸热反应,且随温度升高 ΔHhydr增大,等压比热容cp为 0.2126kJ/(mol·K);ACE 催化 HHL 的水解反应符合 Michaelis-Menten 机理,在实验温度范围内(298.15~313.15K),米氏常数Km随温度升高而减小,催化常数kcat随温度的升高先增大后减少,在308.15K时达到最大值2.534s−1。将该法与传统的初始速率法进行比较,传统法存在的局限性使测得的 Km相对偏大。 药物筛选:快速评估候选药物与靶标蛋白的结合特性,指导药物优化; 抗体研究:解析抗体-抗原相互作用的动力学与热力学机制; 酶动力学分析:精确测定酶促反应速率及抑制剂效应; 纳米材料表征:研究纳米颗粒与蛋白质的吸附机制,揭示材料生物相容性; 电池研发:分析电极材料的热行为,优化储能设备性能。 等温滴定量热仪(ITC)作为精准解析分子相互作用热力学参数的核心工具,在生物医药、纳米材料及制剂研发中展现出不可替代的应用价值。可精确获取结合常数(Ka)、解离常数(Kd)、焓变(ΔH)和熵变(ΔS)等参数,为药物配方优化提供数据支撑。在辅料筛选中,ITC可定量表征表面活性剂与蛋白药物的结合特性,揭示辅料浓度对药物稳定性的调控机制。使其成为解析分子作用机制、优化工业制剂的核心工具,并推动生物医药和材料科学领域的创新突破。 [1] 王宁.分子光谱和等温滴定量热法研究蛋白与小分子的相互作用[D].郑州大学,2019. [2]彭尚,孙丽霞,熊珍爱,等.等温滴定量热法测定酶催化反应的热动力学参数[J].化工进展,2016,35(11):3459-3464.DOI:10.16085/j.issn.1000-6613.2016.11.011. 本文来自:瑞科和利 | 产品分类
重点推荐产品
|