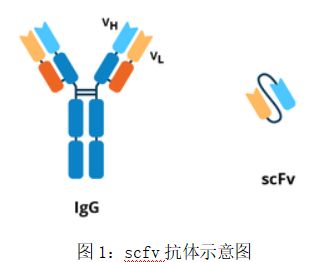
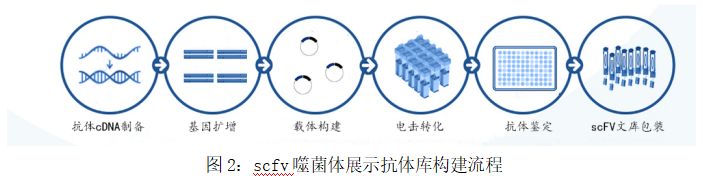
scfv抗体噬菌体展示流程
作者:卡梅德生物 2023.06.20 点击568次
1.什么是scfv抗体文库 噬菌体展示文库是将外源蛋白或多肽与噬菌体外壳蛋白融合,展示在噬菌体表面并保持特定的空间构象,利用特异性亲和作用以筛选特异性蛋白或多肽的一项新技术。 Single-chain Fv(scFv)片段由抗体的最小功能性抗原结合结构域 (~30 kDa) 组成,其中可变重链 (VH) 和可变轻链 (VL) 通过肽接头连接在一起。抗体文库是指将抗体的可变区(VH和VL)基因,尤其是CDR区域(互补决定区)采用不同的策略和方式,如氨基酸突变,移码读框等形成数目庞大的不同克隆,并从这些克隆中筛选出针对目的抗原的高亲和力单链Fv抗体。
3.scfv抗体文库优点 ScFv 片段保留了亲本抗体的结合特异性,与全长 mAb 相比具有多项优势。 (1)具有药代动力学特性,例如更好的组织渗透和快速的血液清除,有利于放射治疗和诊断应用。例如,与完整抗体相比,这些片段可以更快地渗透到肿瘤中;当 scFv 在放射治疗应用中与放射性核素结合时,它们从血液中清除率增加最大限度地减少了健康组织的暴露。 (2)重组抗体缺少 Fc 区,导致免疫原性低,因此与全长 mAb 相比,它们在许多应用中成为更好的治疗剂。 (3)scFv 可以在细菌和哺乳动物细胞中克隆和表达,从而可以轻松且经济高效地大量生产。
4.scfv抗体文库应用 scfv抗体在人类生命科学发展历程中发挥着重要作用。例如作为工具研究蛋白质功能 ,癌症治疗,由于尺寸较小可以与量子点、纳米粒子结合,可以进入体内定位目标,作为运载药物/纳米粒子的载体等。5.scfv抗体文库构建的全流程介绍 scfv噬菌体文库构建服务,流程包括:抗体cDNA制备,基因扩增,载体构建,电击转化,抗体鉴定,scfv文库包装。 5.1抗体cDNA制备 5.1.1总RNA提取 将外周血淋巴细胞从冰箱取出后分装,加入氯仿,离心后取上清加入异丙醇,离心保留沉淀,加入75%乙醇后离心保留沉淀,干燥后加入DEPC水,孵育确保RNA溶解,将各管混合到一管中即为总RNA,取1μl总RNA进行电泳,取2μl用核酸浓度测量仪测浓度。
5.1.2反转录获取cDNA 按照商业化试剂盒操作说明书进行cDNA制备,将上一步得到的RNA一分为二反转录成cDNA,反转录引物分别用Oligo dTprimer及random 6-mers。
5.2 基因扩增 首先,以cDNA为模板扩增VH和VL(Vκ/Vλ)链可变区,进行两轮PCR扩增。PCR反应(每个50μl)包含2μlcDNA (40 ng/μl)、1μl正向引物 (10μM)、1μl反向引物 (10μM)、0.5μl Q5 DNA 聚合酶, 1μl dNTP 混合物 (10μM) 和34.5μl dd H2O.然后,回收 PCR 产物。最后,通过重叠 PCR 连接 VH 和 VL 接头。
5.3载体构建 PCR扩增产物scFv通过酶切连接到噬菌体质粒pADL-10b中,从而构建含有扩增片段的噬菌体质粒库。将连接产物使用DNA纯化回收试剂盒按说明书回收,分别取2μl用核酸浓度测量仪检测回收产物的浓度。
5.4电击转化 5.4.1将连接产物进行电击转化后构建含有目的抗体片段的大肠杆菌文库。 取SS320大肠杆菌感受态细胞,加入回收后的连接产物,将混合后的感受态细胞和连接产物转移到预冷好的电转杯中,使用电转仪预设的转化程序电击转化,电转后立即往电转杯中加入950μlSOC培养基,至少进行20个电转。将细胞复苏后涂在含有氨苄抗性的琼脂糖培养板上过夜生长。将上一步过夜生长后的培养板上的细胞用2xYT培养基和涂布棒冲洗刮下,加入20%的甘油测OD600nm值后保存在-80℃,即为细菌文库。 5.4.2噬菌体文库扩增 将上一步刮下的菌体混匀后转移到100 mL预先加入四环素的2x YT培养液中,37℃,250rpm培养直至OD600nm达到0.5-0.55。 按照辅助噬菌体:细菌细胞数目为20:1的比例加入辅助噬菌体后继续37℃培养30分钟。加入终浓度为50μg/mL的Kana和终浓度为0.2mMI PTG,30℃过夜摇床培养。 5.4.3噬菌体文库制备 将过夜培养的细菌4℃ 4000 rpm离心20分钟,将上清转移到新的离心管后加入1/4体积预冷的的20%PEG/2.5M NaCl,在冰上孵育30分钟。4℃ 4000 rpm离心20分钟去除上清后加入1 mL PBS缓冲液溶解沉淀。再次加入1/4 体积预冷的20%PEG/2.5M NaCl后冰上孵育10分钟,4℃ 12000 xg离心10分钟后去除上清并将沉淀溶解在1 mL PBS中得到噬菌体库,长期-80℃保存,短期(1-2周)可于4℃放置保存。
5.5抗体鉴定 随机挑选20-50个克隆,PCR鉴定阳性率,测序和分析抗体序列。
5.6 scfv文库包装 交付>1x1013噬菌体颗粒/ml。
自 1988 年推出以来,scFv 在临床前和临床应用以及研究实验室中变得高度相关。抗体工程的进步使高度定制的 scFv 的产生成为可能,这些 scFv 具有改善药代动力学的特性,使其更具临床相关性。将这些重组抗体与不同粒子偶联,扩大了它们在诊断、治疗和体内成像应用中的潜力。 | 产品分类
|
 |