多能干细胞具有发育的全能性,可在体外分化为各类组织和细胞,颇具应用前景:可作为再生医学中的重要种子细胞,可在药物研究中筛选临床治疗药物,还可在体外模拟发育的过程。由于发育地位特殊,多能干细胞基因组具高度稳态(如小鼠胚胎干细胞的基因组变异率仅为胚胎成纤维细胞的1/100)。然而,多能干细胞在体外长期大量扩增培养、持续的DNA复制及特殊的细胞周期往往导致基因组变异,破坏其分化潜能,并产生致瘤风险,成为多能干细胞广泛应用特别是走向临床应用的瓶颈。研究多能干细胞维持基因组稳态的特殊机制,有助于解决长期大量扩增培养产生的基因组变异难题。
DNA复制是细胞基因组不稳定的主要原因。在遭遇DNA复制障碍时,停顿的DNA复制叉不稳定,易发生坍塌,形成DNA双链断裂。DNA双链断裂(DSB)是严重的DNA损伤形式。错误的DSB的修复,将导致细胞死亡或癌变。为避免复制叉坍塌,细胞可利用低保真的DNA聚合酶REV1直接进行跨损伤DNA合成(Translesion DNA synthesis,TLS)。若细胞遭遇DSB,细胞主要通过三种方式修复DNA——非同源末端连接(nonhomologous end joining,NHEJ)、同源重组修复(homologous recombination,HR)和微同源末端连接修复(microhomology-mediated end-joining,MMEJ)。其中,MMEJ修复途径保真度最差、突变率最高,由Polq基因编码的Polθ介导。面临复制压力的胚胎干细胞如何避免低保真的DNA复制和修复方式,维持极高的基因组稳态,其中的机制尚不清楚。
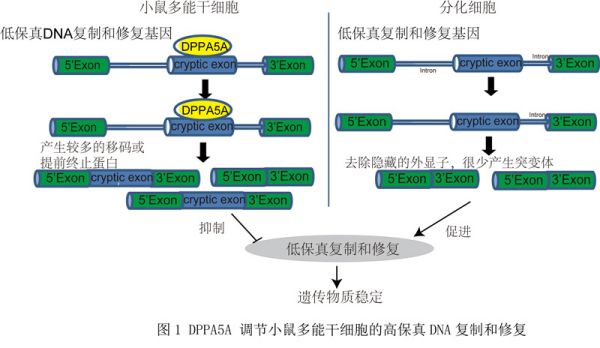
近期,中国科学院昆明动物研究所研究员郑萍团队发现,在小鼠胚胎干细胞中,较多经典的DNA损伤反应基因具有 “隐藏外显子”(cryptic exon)插入事件。“隐藏外显子”的插入导致mRNA翻译提前终止,破坏蛋白翻译和功能。研究聚焦于参与TLS途径的Rev1基因和参与MMEJ途径的Polq基因。二者在小鼠胚胎干细胞中存在高比例的“隐藏外显子”插入,使得小鼠胚胎干细胞中正常的REV1和POLθ蛋白表达显著降低,从而抑制TLS和MMEJ途径。为找到调节二者的剪接因子,研究体外合成了Rev1的“隐藏外显子”,利用体外RNA-pulldown鉴定了Rev1“隐藏外显子”的结合蛋白DPPA5A(小鼠胚胎干细胞特异表达蛋白)。在小鼠胚胎干细胞中,敲低Dppa5a可减弱Rev1和Polq的“隐藏外显子”插入频率,增强TLS和MMEJ途径的活性,抑制同源重组修复。Dppa5a敲低细胞表现出基因组不稳定的表型,包括非整倍体的细胞增加、染色体发生黏连、易于在体内形成畸胎瘤等。与之相反,在体细胞中过表达Dppa5a表现出相反的表型。机制研究表明,DPPA5A直接结合到Rev1“隐藏外显子”的GA富集区,与剪接复合体中的U2相互作用,促进Rev1的“隐藏外显子”插入。上述研究揭示了多能干细胞保持高保真DNA复制和修复的新机制。
7月17日,相关研究成果以DPPA5A suppresses the mutagenic TLS and MMEJ pathways by modulating the cryptic splicing of Rev1 and Polq in mouse embryonic stem cells为题,发表在《美国国家科学院院刊》(PNAS)上。研究工作得到国家重点研发计划、国家自然科学基金和云南省基础研究计划的支持。