在续航里程焦虑的不断刺激下,液态锂金属电池因其高能量密度而成为关注热点,但锂金属负极的严重失效制约了锂金属电池的商业化发展。目前,学界对锂金属负极失效和保护的机理认知尚存争议。传统观点认为,锂枝晶的生长是金属锂负极失效的主要原因。然而,实际上,尽管文献中报道了无枝晶生长的金属锂负极,但采用高面容量正极(≥ 2 mAh cm-2)和超薄锂负极(如50 μm)的实用型锂金属电池通常会在100个充放循环以内发生容量跳水失效问题,这远不如相同容量下锂离子电池的循环性能。当拆开容量跳水失效的实用型锂金属软包电池时,通常会观察到金属锂负极严重粉化。但目前,学界仍不清楚金属锂负极粉化的起源及其组分。
近年来,中国科学院青岛生物能源与过程研究所固态能源系统技术中心研究员崔光磊、董杉木,在锂金属电池和锂金属负极保护等领域取得了系列研究成果(Chem. Mater. 2017, 29, 4682-4689;Chem. Sci. 2018, 9, 3451-3458;Chem. Mater. 2018, 30, 12, 4039-4047;Angew. Chem. 2019, 131, 5997-6001;Small 2019, 15, 1900269;Chem. Mater. 2020, 32, 8, 3405-3413)。在推进这些工作的过程中,研究人员通过在线差分电化学质谱发现,在充放电过程中,锂金属电池中会产生大量H2,锂金属负极会不会与H2反应形成LiH?LiH会不会是锂金属负极的膨胀粉化失效的罪魁祸首?研究人员把在线差分电化学质谱系统进行升级,实现在线滴定气体分析功能。通过氘水(D2O)滴定金属锂负极(判据:2Li + 2D2O → 2LiOD + D2↑;LiH + D2O → LiOD + HD↑),该研究首次发现,失效粉化的金属锂负极中存在大量导电性差的氢化锂(LiH);实用型锂金属电池(2.805 mAh cm-2 LiCoO2, 50 μm Li)的循环性能与锂金属负极中LiH的积累呈负相关性。该研究揭示LiH的生成和分解由一个温度敏感的化学平衡(Li + 1/2H2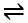 LiH)决定:在室温条件下,界面副反应产生的H2与锂金属反应生成LiH;通过加热,LiH会部分分解产生导电性优异且具有电化学活性的锂金属,从而恢复提升容量。研究表明,有效抑制H2的产生和LiH的积累对锂金属负极的保护具有重要意义,这为实用型锂金属电池的发展提供了新思路:在正极侧,电解液氧化产物R-H+穿梭到负极还原是H2产生的主要原因,通过钝化正极和配制含氢少的电解液两种策略抑制R-H+的产生;通过隔膜或聚合物电解质的功能化处理阻止R-H+穿梭到负极;在金属锂负极构建储氢或吸附氢能力强的界面保护材料,实际上,目前报道的能够有效保护金属锂负极的界面组分(如LiF、 Li3N、BN、Li2O和纳米碳材料等)均是优异的储氢材料;采用加热加压策略。此外,研究人员提示,应该在各类电池体系中,加强电极界面上金属氢化物的表征研究,这将开创电池界面研究的新方向。
LiH)决定:在室温条件下,界面副反应产生的H2与锂金属反应生成LiH;通过加热,LiH会部分分解产生导电性优异且具有电化学活性的锂金属,从而恢复提升容量。研究表明,有效抑制H2的产生和LiH的积累对锂金属负极的保护具有重要意义,这为实用型锂金属电池的发展提供了新思路:在正极侧,电解液氧化产物R-H+穿梭到负极还原是H2产生的主要原因,通过钝化正极和配制含氢少的电解液两种策略抑制R-H+的产生;通过隔膜或聚合物电解质的功能化处理阻止R-H+穿梭到负极;在金属锂负极构建储氢或吸附氢能力强的界面保护材料,实际上,目前报道的能够有效保护金属锂负极的界面组分(如LiF、 Li3N、BN、Li2O和纳米碳材料等)均是优异的储氢材料;采用加热加压策略。此外,研究人员提示,应该在各类电池体系中,加强电极界面上金属氢化物的表征研究,这将开创电池界面研究的新方向。
近日,相关研究成果发表在Angewandte Chemie International Edition上,青岛能源所固态能源系统技术中心教师许高洁、李杰东、王超为论文的共同第一作者,崔光磊、董杉木为论文通讯作者。研究工作得到国家重点研发计划、中科院战略性先导科技专项、国家杰出青年科学基金,中科院青年创新促进会、山东省重点研发计划等的支持。
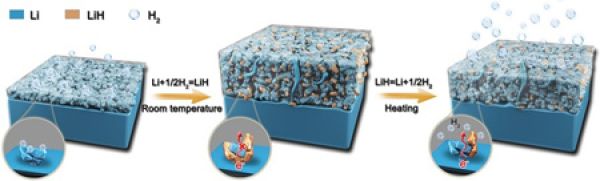
青岛能源所提出实用型锂金属电池失效新机制及优化新思路